Umfassende Nachsorge von Patienten mit Hüfttotalprothesen mit Pfannen mit doppelter Beweglichkeit.
Gemeinsame Informationsschrift über die SNDS-Post-Registrierungsstudie für die umfassende Nachsorge von Patienten mit Hüft-Totalprothesen mit Pfannen mit doppelter Beweglichkeit (EPI CDM-HPT).
In Übereinstimmung mit den Bestimmungen von Artikel 14 der DSGVO beschreibt dieser Hinweis auf kollektive Informationen die Maßnahmen, die im Rahmen von Studien durchgeführt werden, die keine individuellen Informationen zulassen und die den Zugang zu Daten aus dem Nationalen System der Gesundheitsdaten (SNDS) erfordern.
- Verantwortlich für die Verarbeitung :
X.NOV MEDICAL TECHNOLOGY SA mit Sitz in Rue d'Airmont 7, CH-2900 PORRENTRUY, vertreten durch ihren europäischen Bevollmächtigten X. NOV mit Sitz in 14 rue du Chêne sec, - ZAC les Guinnottes 2, 70400 HERICOURT, eingetragen im Handels- und Gesellschaftsregister von VESOUL unter der Nummer 448 101 626, führt eine Studie durch, die vom Comité d'Expertise pour les Recherches, les Etudes et les Evaluations dans le domaine de la Santé (CESREES) am 10. Dezember 2020 als von öffentlichem Interesse bewertet wurde (weitere Informationen zu diesem Thema finden Sie auf der Seitehttps://www.health-data-hub.fr/outil-de-visualisation). Diese Studie wird an IQVIA Opérations France mit Sitz in 17 bis Place des Reflets 92400 Courbevoie, eingetragen im Handelsregister von Nanterre unter der Nummer 347 939 415, delegiert, die für die Durchführung der Verarbeitung verantwortlich ist.
- Kontaktdaten des DPO, des Vertreters des für die Verarbeitung Verantwortlichen : eu.dpo@iqvia.com
- Finalités :
Das Hauptziel ist die Quantifizierung und der Vergleich der Gesamtüberlebensraten von Hüftprothesenträgern (Dauer der Implantation ohne Revision) und der Luxationsraten in der Gruppe mit doppelt beweglichen Pfannen im Vergleich zu einfach beweglichen Pfannen, insgesamt und in Abhängigkeit von den Risikofaktoren für eine Revision in einer nationalen Studie nach der Registrierung.
Rechtsgrundlage : Gemäß Artikel 6 der DSGVO und Artikel 5 des Gesetzes über Informatik und Freiheiten beruht die Verarbeitung im Rahmen dieser Studie auf öffentlichem Interesse mit dem Ziel der Forschung, Studien, Bewertung und Innovation im Gesundheitswesen. Diese gemeinsame Studie von etwa 20 Herstellern wurde auf Antrag der CNEDiMTS (Stellungnahme vom 24. Januar 2017) für die Erneuerung der Aufnahme dieser Produkte in die Liste der erstattungsfähigen Produkte und Leistungen eingerichtet.
Gemäß Artikel 9 der DSGVO dient die Verarbeitung dieser personenbezogenen Gesundheitsdaten wissenschaftlichen Forschungszwecken.
Am 2. April 2020 teilte das Comité Ethique et Scientifique pour les Recherches, les Etudes, et les Évaluations en Santé (CESREES) mit, dass die Studie von öffentlichem Interesse sei (Nummer 1502850).
Die Studie wurde von der CNIL gemäß Artikel 66 des Gesetzes Nr. 78-17 „Informatique et Libertés“ vom 6. Januar 1978 in der geänderten Fassung genehmigt (Entscheidung DR-2020-210; 10. Juli 2023).
- Verwendete SNDS-Datenkategorien :
Daten aus den Datenbanken Daten aus den Datenbanken SNIIRAM (Système National d'Information Inter Régimes de l'Assurance Maladie), PMSI (Programme de Médicalisation des Systèmes d'Information), die von der nationalen Krankenkasse (CNAM) zwischen dem 01/01/2012 und dem 31/12/2023 gehalten werden.
Die Daten, die im SDNS verarbeitet werden, sind Daten über Krankenhausaufenthalte (Krankheit, die für den Krankenhausaufenthalt verantwortlich war, und damit verbundene Komorbiditäten) und/oder erstattete Behandlungen, die in der Stadt durchgeführt wurden (Arztbesuch, Verabreichung von Behandlungen, medizinische Handlungen, ...), sowie soziodemografische Daten (Alter/Geburtsjahr, Geschlecht ...).
Gemäß dem Code de la Santé Publique (CSP) können die in diesen Datenbanken enthaltenen persönlichen Daten nicht zur Identifizierung der Personen verwendet werden, auf die sie sich beziehen.
- Dauer der Datenspeicherung: 3 Jahre nach der Bereitstellung.
- Verantwortlich für die Durchführung der Verarbeitung und Empfänger der Daten :
Die Daten werden von der CNAM auf dem gesicherten IT-Portal der CNAM für den ernannten Implementierungsmanager IQVIA zur Verfügung gestellt.
- Datenübertragung: Diese Daten werden nicht außerhalb der Europäischen Union übertragen.
- Geltendmachung von Rechten und Beschwerden :
Gemäß der DSGVO und dem französischen Datenschutzgesetz haben Sie grundsätzlich ein Recht auf Zugang, Berichtigung, Einschränkung und Löschung Ihrer im Rahmen der Studie verarbeiteten Daten, das Sie gegenüber dem Datenschutzbeauftragten von IQVIA Opérations France, Frau Barbara BRESSOLLES, unter folgender Adresse geltend machen können eu.dpo@iqvia.com.
Wir erinnern Sie daran, dass für den allgemeinen Einspruch gegen jede Weiterverwendung von SNDS-Daten die Bestimmungen von Artikel R 1461-9 des CSP über die Modalitäten der Ausübung von Rechten vorsehen, dass das Recht auf Zugang, Berichtigung und Einspruch bei der Direktion der Plattform für Gesundheitsdaten (Health Data Hub) ausgeübt werden kann, https ://www.healthdata-hub.fr/contact) oder an den Direktor des Trägers der gesetzlichen Krankenversicherung, bei dem Sie versichert sind.
Sie haben auch das Recht, eine Beschwerde bei der Commission Nationale de l'Informatique et des Libertés (CNIL) online oder per Post an CNIL - Service des Plaintes - 3 Place de Fontenoy - TSA 80715 - 75334 PARIS CEDEX 07 einzureichen.





 auf den Etiketten Ihrer Implantatkarte. Lesen Sie dann die entsprechende Zeile, um die Lebensdauer zu erfahren.
auf den Etiketten Ihrer Implantatkarte. Lesen Sie dann die entsprechende Zeile, um die Lebensdauer zu erfahren. auf Ihren Etiketten.
auf Ihren Etiketten. 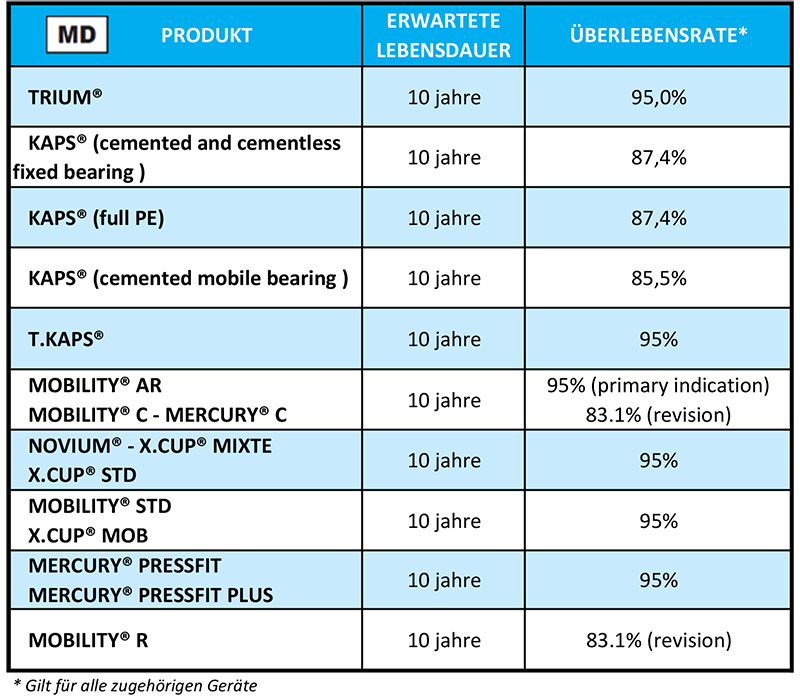
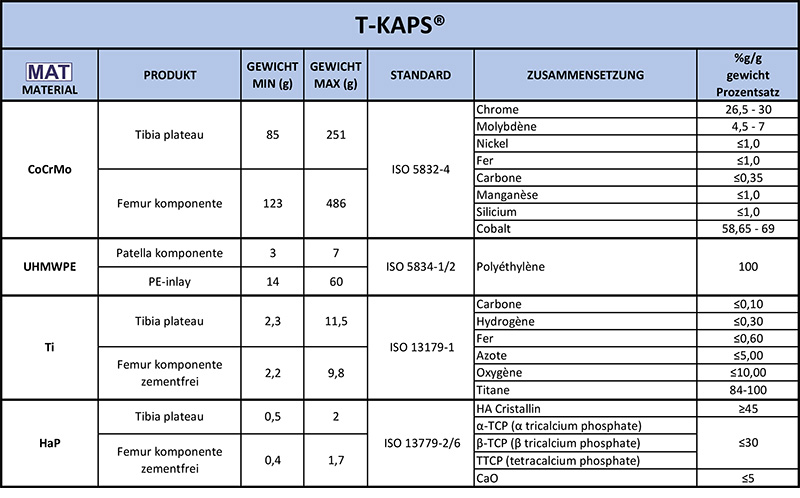
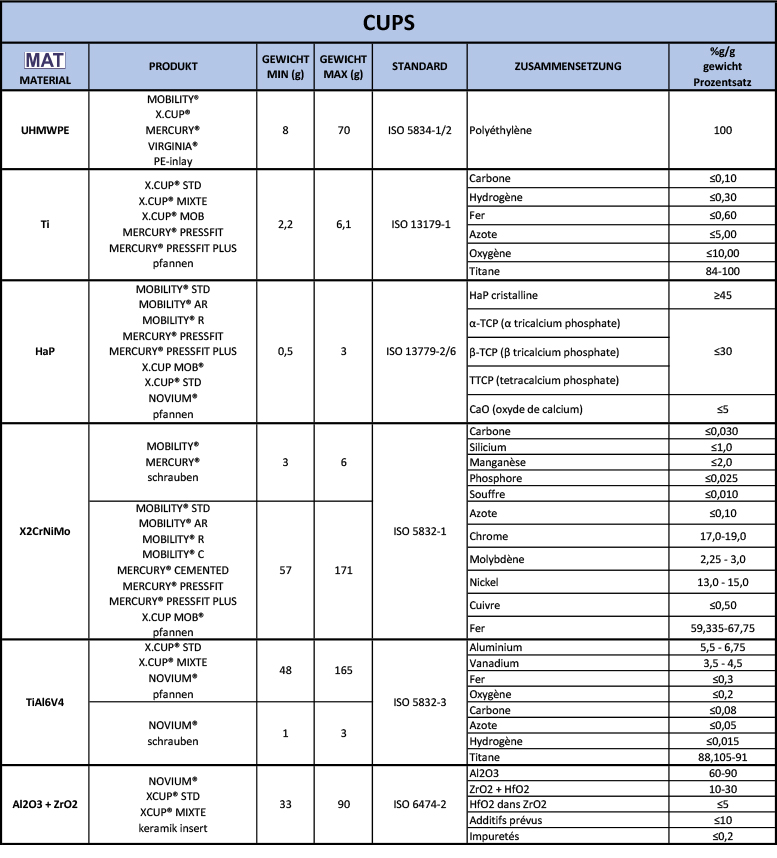
 auf den Etiketten Ihrer Implantatkarte. Lesen Sie dann die entsprechende Zeile, um die Zusammensetzung zu erfahren.
auf den Etiketten Ihrer Implantatkarte. Lesen Sie dann die entsprechende Zeile, um die Zusammensetzung zu erfahren.  Ihrer Etiketten.
Ihrer Etiketten.